Negli anni sono apparsi in letteratura un numero crescente di studi che indagano le funzioni cognitive in pazienti con dolore cronico. I pazienti con dolore cronico non oncologico segnalano spesso difficoltà nella memoria, nella concentrazione e in altre funzioni cognitive rispetto ai pazienti che cercano il trattamento per altri problemi medici.
Federica Aloisio, OPEN SCHOOL STUDI COGNITIVI San Benedetto del Tronto
Il dolore cronico
Il dolore è un fenomeno individuale e soggettivo che le persone sperimentano durante la propria vita e, spesso, rappresenta la ragione principale per cui si richiede assistenza sanitaria.
Per “dolore”, secondo l’International Association for the Study of Pain (IASP), si intende un’esperienza sensoriale ed emozionale spiacevole associata a danno tessutale, in atto o potenziale, o descritta in termini di tale danno.
La maggior parte dei dolori si risolve prontamente una volta che lo stimolo doloroso viene rimosso e l’organismo è guarito ma, se la malattia si prolunga o non regredisce completamente, il dolore persiste diventando cronico.
Il dolore cronico è stato generalmente definito come il dolore che persiste per un periodo di tempo specifico già determinato arbitrariamente (per es. 3 o 6 mesi, oppure al di là del periodo normale di guarigione). “Il dolore cronico invalidante è uno dei maggiori problemi socio-sanitari di proporzioni epidemiche; è la causa più frequente di sofferenza e di invalidità (menomazione) capace di danneggiare seriamente la qualità di vita” (Loeser, 2002).
Secondo i principali e più accreditati studi epidemiologici internazionali la presenza delle sindromi dolorose croniche varia tra 10,1% e 55,2% della popolazione; mediamente, essa è più elevata tra le donne che fra gli uomini, rispettivamente 39% e 31%, e aumenta con l’età, soprattutto dopo i 65 anni (Breivik et al., 2006).
Nella maggior parte dei pazienti, il dolore influisce negativamente sulla percezione della salute generale, interferisce notevolmente con le attività quotidiane, è associato a sintomi depressivi e/o ansiosi ed influenza negativamente i rapporti e le interazioni con gli altri (Froud et al., 2014). Proprio per questi motivi è necessaria una valutazione globale e una presa in carico della persona nella sua complessità.
Le funzioni cognitive nei pazienti con dolore cronico
Negli anni sono apparsi in letteratura un numero crescente di studi che indagano le funzioni cognitive in pazienti con dolore cronico.
I pazienti con dolore cronico non oncologico segnalano spesso difficoltà nella memoria, nella concentrazione e in altre funzioni cognitive rispetto ai pazienti che cercano il trattamento per altri problemi medici.
Grigsby e colleghi nel 1995 hanno confrontato le prestazioni di pazienti con dolore cronico con pazienti senza dolore su una varietà di compiti informatici progettati per valutare la velocità di elaborazione delle informazioni e la memoria a breve termine. I ricercatori hanno scoperto che i pazienti con dolore cronico avevano scarse performance rispetto all’altro gruppo (Grigsby et al., 1995). In un altro studio, il 54% dei pazienti inviati ad un centro di dolore hanno riferito problemi in alcune funzioni cognitive, quali la memoria a breve termine, la concentrazione e l’attenzione (McCracken & Iverson, 2001).
Lo studio di Schiltenwolf conferma il calo nella prestazione in prove di attenzione nei pazienti con lombalgia cronica (Schiltenwolf et al., 2014); queste alterazioni sono risultate anche in pazienti con fibromialgia: oltre il 50% dei pazienti con fibromialgia lamentano disturbi mnestici, di concentrazione e confusione mentale (Dick et al., 2002; Katz et al., 2004).
Inoltre i pazienti con dolore cronico riportano difficoltà nelle funzioni cognitive, quali l’apprendimento percettivo e la memoria, evidenziando alterate capacità di esecuzione dei compiti, rispetto ai gruppi di controllo (Oosterman et al., 2010).
I pazienti con dolore cronico hanno riportato anche uno scarso rendimento rispetto ai controlli sulle misure di screening cognitivo generale, come l’esame al Mini Mental State Examination (MMSE) (Oosterman et al., 2010). Da diversi dati di letteratura emerge infatti che la prevalenza di deficit cognitivo clinicamente rilevante è più alta in pazienti con dolore cronico rispetto alla popolazione generale (Rodriguez-Andreu et al., 2009).
Anche le funzioni esecutive risentono del dolore cronico. La funzione esecutiva definisce quei processi neurologici che consentono compiti cognitivi più complessi, quali la pianificazione, l’organizzazione, il controllo dei pensieri contrastanti, il comportamento diretto ad uno scopo, l’inizio di un’azione e il saper valutare le conseguenze delle azioni. Le performance dei pazienti con dolore cronico sembrano dimostrare che il controllo delle funzioni esecutive risente di questa tipologia di dolore (Moriarty et al, 2011).
Lo studio di Simons ha evidenziato che, da studi di imaging cerebrale in pazienti con dolore e in modelli di roditori, il dolore cronico è associato ad alterazioni anatomiche e funzionali nel cervello.
I ricercatori hanno infatti riscontrato che, come il dolore può causare deficit nei processi cognitivi degli esseri umani, altrettanto avviene nei roditori. Quest’ultimi possono eseguire una serie di prove che coinvolgono le “funzioni esecutive”, come la funzione decisionale, la memoria, l’attività di attenzione e il riconoscimento di oggetti, proprio come gli esseri umani e, inoltre, queste attività si basano su analoghe aree corticali prefrontali. E’ stato dimostrato che nei roditori, allo stesso modo degli esseri umani, il dolore interrompe i compiti di memoria di lavoro (Cardoso-Cruz et al., 2013).
Ricerche algologiche hanno individuato l’esistenza di connessioni tra le aree che trasmettono il dolore nel sistema nervoso centrale e la neurobiologia del dolore. Recenti scoperte neurobiologiche hanno infatti riscontrato nel dolore cronico un alterato biochimismo cerebrale locale ed una riorganizzazione corticale funzionale come conseguenza di processi di neuroplasticità. Gli studi morfo-metrici nel dolore cronico effettuati con la morfometria voxel (VBM), una tecnica di risonanza magnetica, indicano l’importanza della neuroplasticità nel dolore cronico.
Immagini di risonanza magnetica in diversi tipi di pazienti con dolore cronico mostrano che il cervello di questi individui è diverso rispetto a quelli di soggetti sani di controllo (Simons et al., 2014). L’anomalia più marcata, osservata attraverso gli studi, è una riduzione della materia grigia soprattutto nella corteccia prefrontale, nell’insula e nelle cortecce anteriore e nella metà del cingolo (Davis & Moayedi, 2013). Questa perdita è correlata con la durata del dolore cronico e spesso si normalizza con il trattamento.
Kuchinad e colleghi hanno individuato che nei pazienti fibromialgici c’è una perdita di sostanza bianca molto più importante rispetto ai controlli; inoltre ogni anno di fibromialgia corrisponde a 9,5 volte la perdita di sostanza grigia del normale invecchiamento (Kuchinad et al., 2007).
Apkarian nel 2004 ha condotto uno studio in cui ha individuato che i pazienti con lombalgia cronica hanno mostrato una riduzione del 5-11% del volume della materia grigia neocorticale rispetto ai soggetti di controllo privi di dolore cronico. L’entità di questa diminuzione è equivalente al volume della materia grigia perso in 10-20 anni di invecchiamento normale (Apkarian et al., 2004). Il volume diminuito è legato alla durata del dolore, ed indica una perdita di 1,3 cm di materia grigia per ogni anno di dolore cronico. La densità della materia grigia è stata ridotta nella corteccia prefrontale dorsolaterale bilaterale e nel talamo destro. I risultati dello studio di Apkarian implicano che il dolore cronico alla schiena è accompagnato da atrofia cerebrale e suggeriscono che la fisiopatologia del dolore cronico comprende i processi talamocorticali (Apkarian et al., 2004).
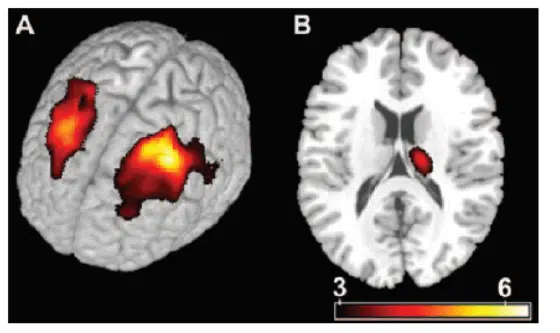
L’immagine seguente, tratta dallo studio di Apkarian, mostra una perdita di densità della materia grigia nei soggetti con lombalgia cronica. Nella figura A si evidenzia che la densità della materia grigia è bilateralmente ridotta. La figura B mostra un significativo decremento della densità della materia grigia nel talamo anteriore destro (Apkarian et al., 2004).
Sulla stessa scia, una metanalisi del 2008 ha evidenziato che il dolore cronico può cambiare la struttura del cervello (May, 2008). I pazienti affetti da mal di schiena cronico, sindrome dell’intestino irritabile, fibromialgia, dolore da arto fantasma e cefalea tensiva cronica presentano alterazioni morfologiche cerebrali di tipo atrofico in alcune specifiche aree deputate alla percezione, all’elaborazione e alla modulazione del dolore. Queste alterazioni, attribuibili a fenomeni di neuroplasticità, sono state riscontrate nel giro cingolato, nella corteccia orbito-frontale, nell’insula e nella regione dorsale del ponte. Poiché sembra che i pazienti affetti da dolore cronico abbiano questa comune “impronta cerebrale” in aree coinvolte nella regolazione del dolore, ci si chiede se questi cambiamenti siano la causa o la conseguenza del dolore cronico.
Secondo May queste modifiche strutturali possono rappresentare il substrato neuro-anatomico della memoria del dolore. L’autore suggerisce che i cambiamenti della materia grigia osservati siano la conseguenza dei frequenti input nocicettivi che sono transitori all’inizio della sindrome dolorosa e poi diventano permanenti con il persistere della malattia ma che potrebbero essere reversibili a seguito di un’idonea terapia antalgica (May, 2008).