Nella malattia di Alzheimer, molte aree cerebrali vanno incontro a deterioramento. Gli studi sul corpo calloso, in particolare, risultano fondamentali. La correlazione tra il deterioramento di tale struttura cerebrale e le manifestazioni psichiatriche e cognitive potrebbe rivelarsi importante per determinare l’inizio della fase prodromica della demenza di Alzheimer.
Luz Dary Grossi
Introduzione: la malattia di Alzheimer
La malattia di Alzheimer è il tipo di demenza più diffuso. Tale disturbo neurodegenerativo è caratterizzato da progressivo deterioramento cognitivo spesso associato a severe manifestazioni psichiatriche.
Gli esami clinici giocano un ruolo fondamentale nella valutazione e nella diagnosi del paziente affetto dalla patologia in questione. Le tecniche di neuroimmagine funzionali e strutturali sono, invece, importanti per lo studio dei cambiamenti cerebrali successive all’insorgere della demenza. La combinazione delle valutazioni neuropsicologiche e neuropsichiatriche con le tecniche di neuroimmagine potrebbe portare, in futuro, a risultati interessanti nella ricerca sulla malattia di Alzheimer.
Nel suddetto disturbo, molte aree cerebrali vanno incontro a deterioramento, coinvolgendo sia la sostanza grigia sia la sostanza bianca all’interno del cervello. In quest’ultimo caso, gli studi sul corpo calloso risultano fondamentali. La correlazione tra il deterioramento di tale struttura cerebrale e le manifestazioni psichiatriche e cognitive potrebbe rivelarsi importante per determinare l’inizio della fase prodromica della malattia di Alzheimer.
Caratteristiche generali della malattia di Alzheimer
La malattia di Alzheimer è una demenza. La demenza o deterioramento cognitivo cronico-progressivo è una conseguenza comportamentale di una patologia acquisita con andamento ingravescente, in cui il declino delle funzioni cognitive interferisce con le attività della vita di tutti i giorni (Vallar e Papagno, 2011).
La demenza di tipo Alzheimer è caratterizzata da una modalità di esordio subdolo e insidioso. Il decorso della malattia di Alzheimer è graduale e progressivo con declino delle facoltà cognitive, le quali si ripercuotono pesantemente sullo stile di vita, sull’autonomia e sulla sfera sociale della persona affetta.
La diagnosi di questo tipo di demenza è effettuata per esclusione, ossia quando i deficit cognitivi non caratterizzano altre condizioni patologiche del sistema nervoso centrale o non sono attribuibili agli effetti di una o più sostanze. La diagnosi è probabilistica e la sua certezza è raggiungibile soltanto attraverso l’esame post- mortem del cervello, evidenziando la presenza di placche senili e degenerazione neurofibrillare. L’accuratezza della diagnosi, tuttavia, risulta essere piuttosto soddisfacente grazie alla combinazione degli esami clinici, di neuroimmagine e soprattutto neuropsicologici.
La malattia di Alzheimer è stata descritta per la prima volta nel 1906. Lo psichiatra e neuropatologo tedesco Alois Alzheimer descrive il caso di una sua paziente, Auguste Deter, la quale presentava segni di decadimento cognitivo, allucinazioni e perdita delle competenze sociali. L’esame autoptico post-mortem della paziente, rivelò il quadro istopatologico caratteristico di questa malattia, ossia la presenza di grovigli neurofibrillari e placche amiloidi.
Epidemiologia
La malattia di Alzheimer è il tipo di demenza più diffuso, rappresentando il 50-70% dei casi. La prevalenza interessa la popolazione al di sopra dei 65 anni di età con maggior incidenza nelle donne; l’età di esordio può raggiungere i 45 anni.
Eziopatogenesi
L’eziopatogenesi della malattia di Alzheimer, ancora oggi, non è del tutto chiara e definitiva. Le diverse ipotesi formulate mettono in evidenza diversi fattori che possono interagire tra loro. Tra questi, ad esempio, i fattori genetici, l’invecchiamento, agenti tossici e fattori vascolari.
Fattori di rischio
I fattori di rischio della malattia di Alzheimer sono:
- l’avanzamento dell’età;
- il genotipo della Apoliproteina E (ApoE);
- sesso femminile;
- bassa scolarità.
I fattori di protezione malattia di Alzheimer sono:
- alto livello d’istruzione;
- svolgimento della regolare attività fisica;
- limitato consumo di alcolici;
- dieta mediterranea.
I fattori prognostici della malattia di Alzheimer sono:
- età di esordio (un esordio precoce è correlato a un’evoluzione più rapida);
- precoce comparsa di segni extrapiramidali;
- manifestazioni psicotiche;
- disturbi del linguaggio (confermato fattore predittivo dell’evoluzione).
Cambiamenti cerebrali nella malattia di Alzheimer
La malattia di Alzheimer è caratterizzata da alterazioni strutturali che colpiscono il cervello. Queste conseguenze cerebrali possono essere considerate microstrutturali e macrostrutturali.
Aspetti microstrutturali
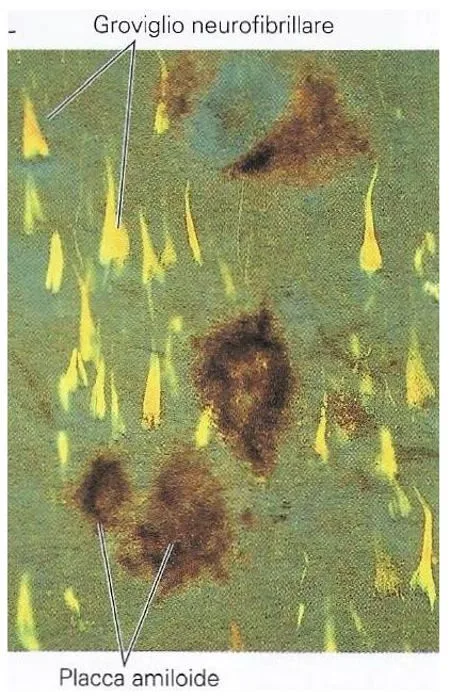
L’esame istopatologico rivela la fondamentale presenza delle placche amiloidi e dei grovigli neurofibrillari (Fig. 1). Nel cervello affetto da Alzheimer queste due lesioni si presentano in misura maggiore e in aree cerebrali diverse rispetto al cervello di soggetti con invecchiamento sano.
Le placche amiloidi sono depositi anomali di un peptide detto β-amiloide. Queste placche si sviluppano nello spazio extracellulare e i neuroni adiacenti ad essi si presentano rigonfi e sformati. La presenza delle cellule della microglia evidenza un tentativo di rimozione delle cellule danneggiate e delle placche amiloidi. Gli studi a livello genetico sono fondamentali poiché il peptide β-amiloide deriva dal taglio di una proteina precursore detta β-APP, la quale viene codificata da un gene localizzato sul cromosoma 21.
I grovigli neurofibrillari sono lesioni che si sviluppano nel citoplasma del neurone. Mutazioni nel gene tau possono modificare il modo in cui la proteina tau si lega ai microtubuli, i quali permettono ai neuroni di trasportare sostanze. Gli intrecci neurofibrilllari sono, dunque, costituiti da depositi fibrosi dovuti ad accumuli intracellulari delle proteine tau anormali.
Aspetti Macrostrutturali
Nel corso degli anni, l’intero corpo umano va incontro a progressivi cambiamenti dovuti all’invecchiamento. Queste alterazioni coinvolgono anche il cervello.
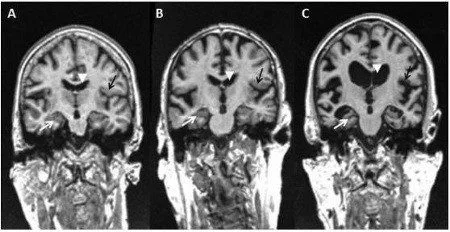
Il normale invecchiamento assume un aspetto fortemente patologico nella malattia di Alzheimer (Fig. 2). La caratteristica cerebrale più importante è l’atrofia dovuta alla perdita progressiva dei neuroni.
Le tecniche di neuroimmagine funzionali e strutturali sono estremamente fondamentali per lo studio della struttura e/o funzionalità del cervello. La tomografia assiale computerizzata (TAC) e la risonanza magnetica per immagini (RMI) evidenziano una riduzione del volume e del peso della sostanza cerebrale nei pazienti affetti dalla malattia di Alzheimer rispetto ai soggetti sani.
L’atrofia, oltre che a condurre ad un allargamento dei solchi cerebrali e ad una dilatazione ventricolare, colpisce soprattutto il lobo temporale mediale. In quest’area l’ippocampo risulta maggiormente danneggiato. L’atrofia ippocampale riflette i deficit mnestici e di disorientamento, caratteristici della demenza di Alzheimer.
La perdita neuronale si verifica anche nella neocorteccia. L’ulteriore atrofia corticale può essere legata a meccanismi di non uso. Infatti, accanto a fenomeni di morte cellulare che interessano in realtà solo un numero limitato di aree cerebrali, il problema forse più serio, per le conseguenze che provoca, è l’atrofia cellulare e la riduzione di attività di cellule nervose ancora vive (Moro e Filippi, 2010).
Cambiamenti cognitivi nella malattia di Alzheimer
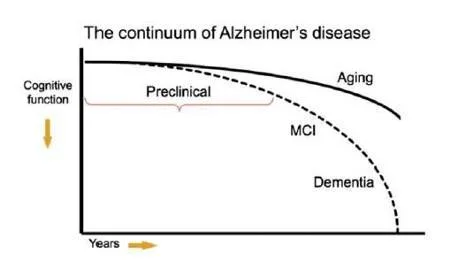
Il quadro cognitivo della malattia di Alzheimer presenta un progressivo deterioramento delle funzioni cognitive. Il disturbo cognitivo che caratterizza maggiormente questo tipo di demenza è il deficit di memoria. Il disturbo è essenzialmente episodico e anterogrado nel senso che il paziente è incapace di apprendere nuove informazioni (Vallar e Papagno, 2011). La memoria prospettica che permette il ricordo di eventi ed azioni da compiere nel futuro è anch’essa notevolmente deficitaria. Uno dei più importanti obiettivi della ricerca sulla malattia di Alzheimer è individuare e definire lo stadio preclinico. I risultati di questi studi potrebbero rivelarsi fondamentali per la diagnosi precoce e per la prevenzione. L’ipotesi attualmente formulata è quella del continuum della compromissione cognitiva (Fig. 3).
La condizione di lieve compromissione cognitiva, nota come Mild Cognitive Impairment (MCI), viene considerata come fase prodromica della malattia di Alzheimer. In questa fase i sintomi cognitivi rilevati non sono né sufficientemente gravi per formulare una diagnosi né dovranno essere sottovalutati. I pazienti con diagnosi di MCI, anche se hanno un maggiore rischio di sviluppare la malattia di Alzheimer, non sempre sfociano in questo quadro patologico. In questo caso, il ruolo della riserva cognitiva risulta fondamentale.
La demenza di Alzheimer può essere divisa in tre fasi evolutive: di esordio, avanzata e tardiva. Nella fase di esordio la sintomatologia non è del tutto chiara. Ad ogni modo, si evidenziano i seguenti deficit:
- disturbi di memoria episodica e anterograda;
- disorientamento temporale e topografico;
- afasia anomica caratterizzata da circonlocuzioni e da parole passepartout;
- difficoltà nel calcolo;
- aprassia costruttiva.
Nella fase avanzata i sintomi sono più definiti. Questo stadio ha un tempo variabile da tre a otto anni circa. I deficit riscontrati sono:
- disturbi di memoria ingravescenti;
- afasia caratterizzata da parafasia, da circonlocuzioni e da difficoltà di comprensione;
- aprassia costruttiva e ideomotoria;
- agnosia;
- alterazioni comportamentali (deliri, allucinazioni e wandering behaviour).
Nella fase tardiva il quadro cognitivo si presenta completamente deteriorato. Si riscontrano:
- perdita completa delle capacità cognitive;
- bradicinesia, rigidità, apatia e aggressività;
- perdita completa dell’autosufficienza e incontinenza sfinterica.
La malattia di Alzheimer non conduce alla morte del paziente. Il decesso avviene per altre cause legate, ad esempio, a problemi respiratori.
Il corpo calloso
Anatomia del corpo calloso
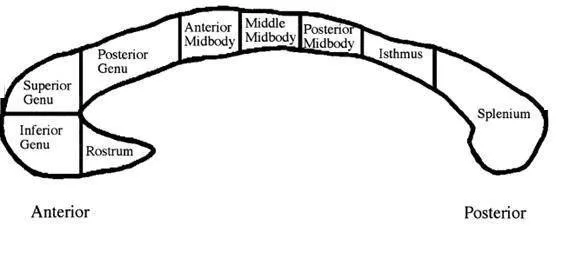
Il corpo calloso appartiene al complesso delle formazioni commissurali interemisferiche costituite da fibre nervose, le quali connettono i due emisferi cerebrali. Il corpo calloso, situato nella scissura interemisferica, si presenta come una lamina di sostanza bianca ad estensione sagittale con curvature in corrispondenza delle sue estremità anteriori e posteriori. Questa struttura presenta le seguenti regioni (Fig. 4):
- il tronco, che costituisce la porzione principale;
- il genu o ginocchio, che costituisce la porzione anteriore ripiegata;
- il rostro, che si trova anteriormente al ginocchio e lo splenio;
- lo splenio, che si trova posteriormente al corpo calloso.
Connessioni callosali
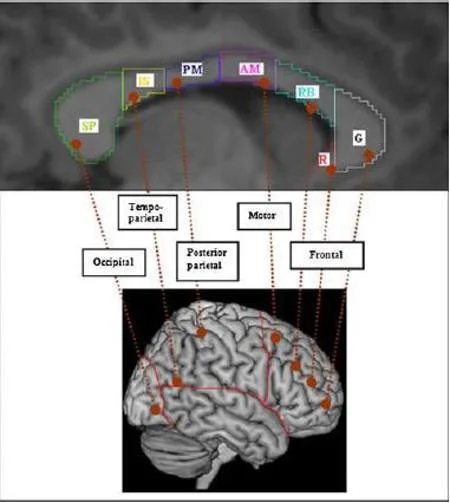
Il corpo calloso connette le aree della neocorteccia di ciascun lato del cervello. Questa unificazione è resa possibile da un grande fascio di assoni che connette le parti corrispondenti dei due emisferi: il lobo temporale sinistro è connesso con il lobo temporale destro; allo stesso modo, il lobo parietale sinistro è connesso con il lobo parietale destro, e così via (Carlson, 2008). Le connessioni callosali, costituite da fasce di fibre mieliniche, sono sia omotopiche che topografiche. Nel primo caso vengono connesse le regioni corticali equivalenti dei due emisferi; nel secondo caso, l’organizzazione topografica delle fibre è tale che la regione anteriore del corpo calloso (rostro e genu) viene attraversata da fibre provenienti dal lobo frontale, mentre la regione posteriore (splenio) è raggiunta da fibre provenienti dalle regioni caudali della corteccia cerebrale (Elahi et al., 2015). Le connessioni del corpo calloso con la corteccia cerebrale sono (Fig. 5):
- rostro e genu (porzione anteriore del corpo calloso) con la corteccia frontale e prefrontale;
- splenio (porzione posteriore del corpo calloso) con la corteccia occipitale, parietale e temporale mediale.
Il corpo calloso e la malattia di Alzheimer
Atrofia del corpo calloso nella malattia di Alzheimer
La malattia di Alzheimer è caratterizzata da molteplici alterazioni che coinvolgono diverse aree del cervello. Molti studi hanno evidenziato deterioramenti cerebrali presenti sia a carico della sostanza grigia, sia a carico della sostanza bianca. In quest’ultimo caso vengono collocate le ricerche effettuate su cambiamenti del corpo calloso nella malattia di Alzheimer. Il corpo calloso è, infatti, il più grosso fascio di fibre di sostanza bianca, le quali sono ricoperte da guaina mielinica. I rivestimenti mielinici assicurano una rapida conduzione del segnale elettrico nel cervello. Questo aspetto è fondamentale nelle fibre callosali, dato il loro coinvolgimento nella trasmissione e integrazione delle informazioni tra i due emisferi cerebrali.
Il deterioramento del corpo calloso associato alla malattia di Alzheimer è stato riportato in studi prevalentemente trasversali. Questo tipo di studi presentano alcune limitazioni; ad esempio, le differenti dimensioni del corpo calloso tra soggetti possono influenzare fortemente la validità dei risultati ottenuti. A tal proposito, gli studi longitudinali presentano più vantaggi rispetto a quelli trasversali. Le tecniche usate per lo studio del corpo calloso sono la Voxel-Based Morphometry (VBM) e la Diffusion Tensor Imaging (DTI). La VBM è particolarmente importante per lo studio dell’intera struttura cerebrale, mentre la DTI è fondamentale per rilevare cambiamenti nelle regioni callosali e nelle guaine mieliniche.
L’atrofia del corpo calloso viene osservata, con maggiore attenzione, nella fase prodromica della malattia di Alzheimer. Molti studi hanno riportato differenze graduali e sostanziali nella struttura callosale tra pazienti con MCI stabile e pazienti con MCI evoluta in demenza. Uno studio longitudinale, ad esempio, ha rivelato simili cambiamenti morfologici e temporali del corpo calloso confrontando soggetti con MCI stabile rispetto al gruppo di controllo. Il dato sorprendente è che questi cambiamenti risultano più veloci e più marcati tra soggetti con MCI evoluta in demenza rispetto a soggetti con MCI stabile (Elahi et al., 2015).
Uno studio di meta- analisi di immagini strutturali ha evidenziato moderate riduzioni del corpo calloso in pazienti con MCI rispetto a pazienti con malattia di Alzheimer. In particolare, i soggetti con MCI presentano atrofia in zone più ristrette del corpo calloso, soprattutto nelle regioni anteriori. Al contrario, soggetti con demenza di Alzheimer hanno un atrofia che coinvolge le regioni anteriori e posteriori del corpo calloso (Xu- Dong Wang et al., 2015). Questi studi citati evidenziano il grado di cambiamento del corpo calloso nella malattia di Alzheimer rispetto a pazienti con MCI. Questo confronto è estremamente fondamentale poiché tale cambiamento callosale potrebbe essere considerato come futuro biomarker, ossia un indicatore che permette di diagnosticare la malattia di Alzheimer.
Meccanismi sottostanti l’atrofia del corpo calloso nella malattia di Alzheimer
L’atrofia del corpo calloso è stata osservata in diverse gravi patologie come la malattia di Alzheimer, schizofrenia, sclerosi multipla e alcolismo. Due possibili meccanismi sono alla base di questa atrofia callosale: la breakdown mielinica e la degenerazione Walleriana (Elahi et al., 2015).
Nel primo caso i differenti tempi di mielinizzazione delle fibre callosali rivestono un ruolo importante. La tarda mielinizzazione viene riscontrata nella regione del rostro, dando luogo a fibre contenenti assoni ridotti. La precoce mielinizzazione, invece, interessa la parte posteriore del corpo calloso, in particolar modo lo splenium. Le fibre con tarda mielinizzazione, essendo più vulnerabili, tendono ad essere le prime a risentire degli effetti dei processi degenerativi. La regione anteriore del corpo calloso, secondo questo meccanismo di mielinizzazione, risulta essere più sensibile a deterioramenti cerebrali dovuti alla malattia di Alzheimer.
Nel secondo caso, l’ipotesi della degenerazione Walleriana suggerisce che la perdita delle fibre callosali è la conseguenza della progressiva perdita di neuroni corticali, i quali inviano proiezioni al corpo calloso.
Atrofia del corpo calloso correlata ad aspetti cognitivi e neuropsichiatrici nella malattia di Alzheimer
Molti studi trasversali e longitudinali hanno confermato la presenza di atrofia del corpo calloso nella fase prodromica della malattia di Alzheimer. Un ulteriore passo avanti della ricerca, è lo studio di una forte correlazione tra il declino del quadro cognitivo e neuropsichiatrico del paziente affetto da demenza di Alzheimer e la degenerazione callosale. In questo caso, la combinazione dell’utilizzo di tecniche di neuroimmagine e di test neuropsicologici e neuropsichiatrici è indispensabile. In questo tipo di ricerca è importante volgere l’attenzione sia ai cambiamenti del corpo calloso sia alle molteplici connessioni che questa struttura instaura con le altre strutture cerebrali.
Uno studio longitudinale condotto per un periodo di un anno ha riportato risultati interessanti (Di Paola et al., 2015). Gli aspetti cognitivi sono maggiormente correlati a un danneggiamento della porzione posteriore del corpo calloso, in particolare l’istmo e lo splenio. Tali regioni sono connesse topograficamente con il lobo temporale e parietale.
Gli aspetti neuropsichiatrici, in particolare la depressione, vengono correlati con un danneggiamento del rostro, la regione posteriore del corpo calloso. Quest’area riceve fibre che originano dalla corteccia orbito frontale, la quale si presenta danneggiata anche in pazienti parkinsoniani che manifestano sintomi depressivi.
Conclusioni
Il corpo calloso è un grosso fascio di fibre che mette in comunicazione gli emisferi cerebrali. Nel corso dell’invecchiamento, questa struttura cerebrale va incontro a graduale deterioramento. Nella malattia di Alzheimer, questo cambiamento callosale risulta essere sia più marcato sia più veloce rispetto a pazienti con MCI.
In soggetti con demenza di Alzheimer, il deterioramento del corpo calloso è piuttosto diffuso, coinvolgendo sia le regioni anteriori (rostro e genu) sia le regioni posteriori (istmo e splenio). La degenerazione Walleriana e la breakdown mielinica potrebbero essere alla base della di questa degenerazione. Le connessioni topografiche del corpo calloso con le diverse regioni cerebrali potrebbero spiegare un collegamento tra questa struttura e le manifestazioni cognitive e psichiatriche del paziente con malattia di Alzheimer. L’atrofia del corpo calloso, studiata in quest’ottica, potrebbe rivelarsi un importante biomarker, il quale consentirebbe di formulare una diagnosi certa di questo tipo di demenza.